肽连接酶(Peptide ligases)是催化骨架酰胺键形成的关键生物催化剂,为肽和蛋白质的合成与修饰必不可少的工具。在已知的肽连接酶中,天冬酰胺多肽连接酶(Peptide Asparaginyl Ligases, PALs)因兼具底物谱广、催化效率高、水解副反应少、产物无痕以及反应条件温和等优势,已成为合成生物学与蛋白质工程领域极具吸引力的生物催化工具。然而,这类酶在自然界中极为罕见,目前已被发现的PALs均来源于能合成环肽的植物,其中超过一半来自堇菜科(Violaceae)的堇菜属(Viola L.)植物。
堇菜属植物富含环肽,本属物种多样且分布广泛,是发掘新型PALs的重要天然资源库。由中国药科大学、中国科学院武汉植物园、浙江药科大学、新加坡南洋理工大学及新加坡科技研究局实验药物开发中心等单位联合组成的研究团队,通过系统的野外调查和种质资源收集,收集了16个此前未开展PALs相关研究的堇菜属物种,连同此前已被研究报道的七个物种,构建了一个涵盖23个堇菜属物种的精选样本库。
通过系统筛选,研究团队从样本库中共鉴定出29个新的PALs,使已知PALs总数扩展至47个。基于双目标筛选策略分析结果,来源于裂叶堇菜(Viola dissecta Ledeb.)的VdiPAL1被鉴定为性能最优的天然PAL,其催化效率为野生型VyPAL2(wt-VyPAL2)的两倍。此外,研究发现VdiPAL1及其同源酶在P2″位点表现出比以往认知更宽的底物耐受性,能够高效识别包括色氨酸、甲硫氨酸、酪氨酸等多种氨基酸残基,显著拓展了其底物适用范围。VdiPAL1的1.8 Å分辨率晶体结构以及恒定pH分子动力学模拟揭示,其活性中心呈现预组织的近攻击构象(Near-Attack Conformation, NAC),为其高效催化活性提供了结构基础。
尽管VdiPAL1与VyPAL2在序列和三维结构上具有高度同源性,VyPAL2在实际应用中却受到表达体系限制,难以满足规模化制备需求。为突破这一瓶颈,研究团队以高表达性的VdiPAL1为模板,对VyPAL2进行结构导向工程改造,获得了五重突变体VyOpt1。该突变体通过增强帽结构域的折叠稳定性,在单轮设计测试循环中实现表达量提升超过24倍,显著提高了其可制备性与应用潜力。
本研究显著丰富了PALs家族资源,揭示了自然多样性在酶发现与优化中的重要价值,并为天然酶的系统挖掘与结构导向改造提供了可借鉴的技术范式。随着更多高性能PALs的发现及应用开发,这一源自植物的生物催化体系有望在生物制药、合成生物学及精准分子修饰等领域发挥更加重要的作用。
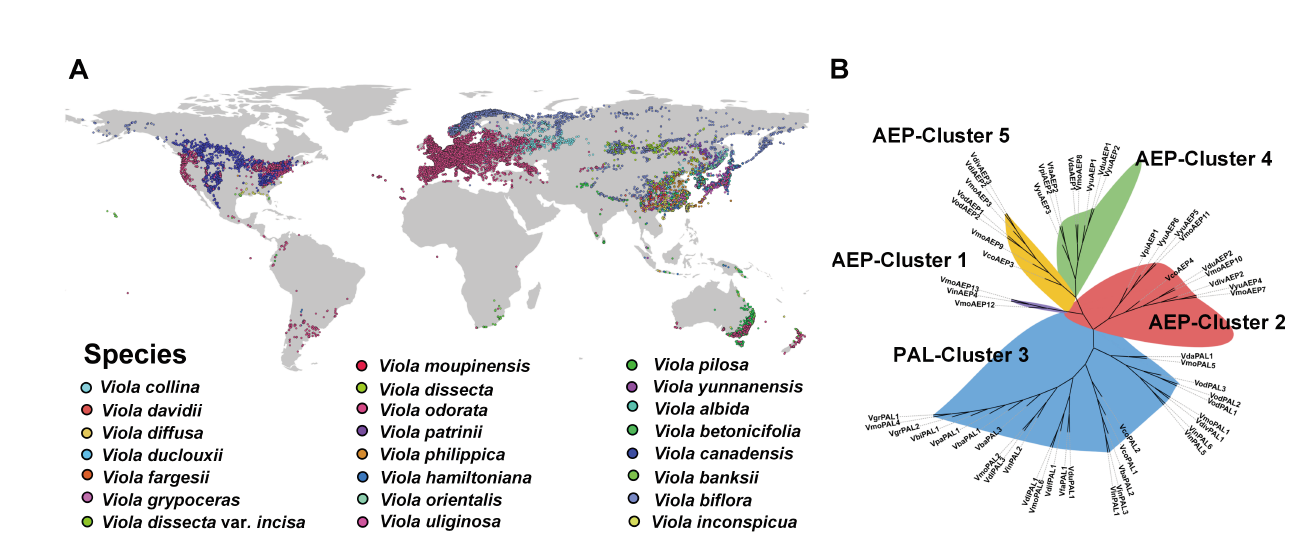
图1. 文中所研究的堇菜属植物及从中新收集的天冬酰胺内肽酶的进化特征。(A) 23种堇菜的地理分布。(B)对57个新收集的天冬酰胺内肽酶(legumain)序列进行系统发育和序列相似性分析,发现一个明显的PAL演化支和4个主要的AEP演化支。
本研究由中国药科大学、中国科学院武汉植物园、浙江药科大学、新加坡南洋理工大学及新加坡科技研究局实验药物开发中心的研究人员合作完成。中国药科大学杜雯煜和齐是为论文共同第一作者,中国药科大学的何牟欣亚教授和武汉植物园胡光万研究员为共同通讯作者,武汉植物园的博士研究生廖苗和江慧参与了研究。该研究获得国家重点研发计划(2023YFA0916000)、国家自然科学基金(32371324、32270228)以及湖北江夏实验室重点研发计划(JXBS010)等项目资助。
相关研究成果以“Mining of natural diversity enables efficient and expressible peptide asparaginyl ligases”为题,发表在国际学术期刊《Nature Communications》上。













